近日,吉林大学化学学院李云峰教授课题组与哈尔滨工业大学齐殿鹏教授合作,在自液化水凝胶粘合剂可编程生物电子界面方面取得了重要进展。水凝胶粘合剂兼具水凝胶和粘合剂的特性,能够牢固地与聚合物、金属、生物组织等多种材料粘合,其广泛应用于伤口敷料、组织修复、药物递送和生物电子等方面。然而,传统的水凝胶粘合剂难以实现在粗糙、多毛发组织表面的有效粘合,因而难以获得高质量的信号,甚至无法采集到信号,此外,水凝胶粘合剂的强行剥离通常会引起电极的损坏和组织损伤。针对这一挑战性科学问题,研究团队创新性地提出一种自液化水凝胶粘合剂策略,结合拮抗酶反应网络驱动的pH调节器,利用硼酯键的可逆形成和断裂实现水凝胶粘合剂的可控形成及自液化,并用于可编程生物电子界面。该工作开拓了化学燃料驱动的瞬态自液化水凝胶粘合剂的应用新方向,推动了下一代具有类生命特性的非平衡水凝胶材料的潜在应用。研究成果以“An Autonomously Liquefied Hydrogel Adhesive for Programmable Bioelectronic Interface”为题,于4月17号发表在Angewandte Chemie International Edition上。
该拮抗酶反应网络驱动的瞬态自液化水凝胶粘合剂包括一下成分:含三羟甲基基团的聚合物P1。含苯硼酸基团的聚合物P2,尿素,脲酶,乙酸戊酯和酯酶。脲酶能够催化尿素生成NH3和CO2,使溶液pH升高,酯酶则催化乙酸戊酯生成乙酸和戊醇,使溶液pH下降,通过调控两种酶催化底物分解的速率,我们能够实现拮抗酶反应网络的pH调控。NH3生成导致的pH值升高能够促进P1的三羟基基团与P2的苯基硼酸基团反应生成动态共价键——硼酯键,瞬态水凝胶粘合剂(THA)形成。随后,AA水解导致的pH降低使得硼酯键水解,水凝胶解体。该粘合剂可作为一种稳定的生物电子界面,用于多毛发皮肤表面实时可编程的粘附和脱离。在拮抗酶反应网络驱动下,瞬态水凝胶粘合剂以时间可编程的方式呈现自主的溶胶-凝胶-溶胶转换(图1)。
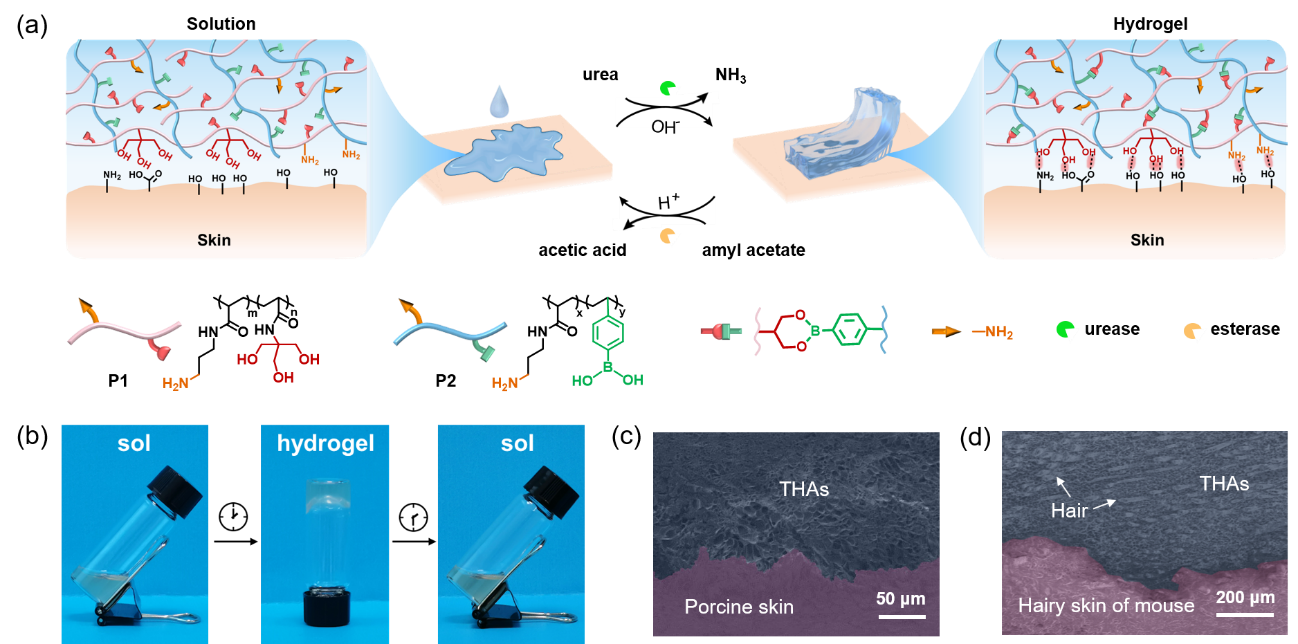
图1.(a)拮抗酶反应网络驱动的瞬态自液化水凝胶粘合剂的示意图;(b)瞬态自液化水凝胶粘合剂自主的溶胶-凝胶-溶胶转换;(c)瞬态水凝胶粘合剂与猪皮表面褶皱的适形粘附扫描电子显微镜照片;(d)瞬态水凝胶粘合剂与小鼠多毛发皮肤的适形粘附扫描电子显微镜照片。
瞬态水凝胶粘合剂的模量和寿命可由拮抗酶反应网络中各组分浓度进行调控。通过分别调节乙酸戊酯、尿素、酯酶和脲酶的含量,水凝胶的力学性能和凝胶寿命能够实现可编程调控(图2)。
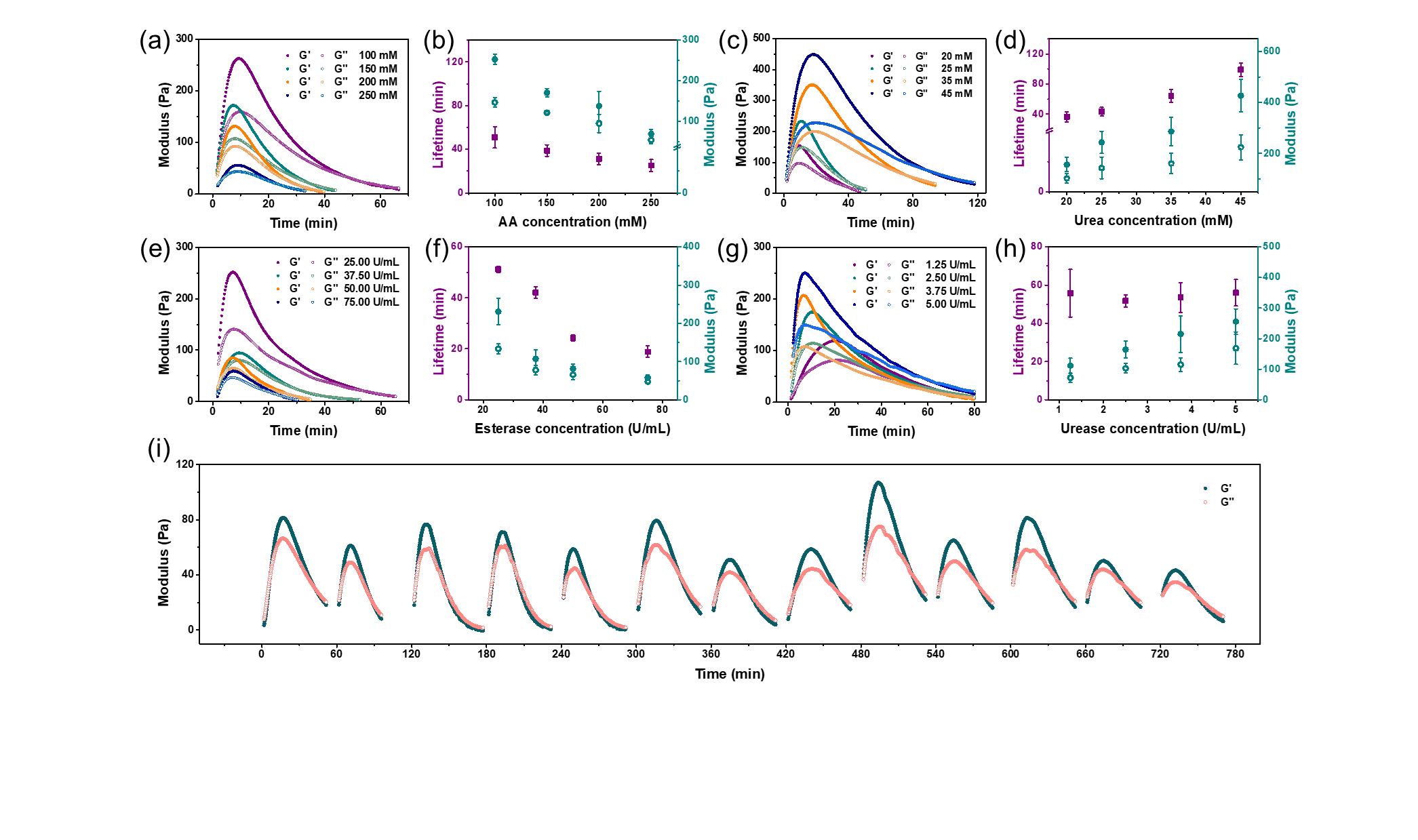
图2.各组分浓度不同时瞬态水凝胶粘合剂模量和寿命的变化。(a、b)改变乙酸戊酯浓度;(c、d)改变尿素浓度;(e、f)改变酯酶浓度;(g、h)改变脲酶浓度。
瞬态水凝胶粘合剂的前体溶液易于穿过毛发区域接触皮肤表面并发生快速的溶胶-凝胶转变,使得生物电极能够适形、稳定地粘附于粗糙、不规则甚至多毛发的皮肤表面。这种适形的生物电子界面结合电极可以在不处理毛发的情况下在多毛发皮肤上直接记录高质量的电生理信号,更重要的是,由于瞬态水凝胶粘合剂的自主液化,使用后的生物电极很容易从皮肤表面剥离,不会造成凝胶的残留,清洗后对多毛发皮肤和电极也没有损伤。传统的商用电极由于毛发阻碍,无法接触到皮肤表面,无法采集有效的电生理信号(图3)。

图3.(a)瞬态水凝胶粘合剂生物电子界面结合电极采集人肌电信号的示意图;(b)不同时间段采集的肌电信号;(c)自液化过程驱动电极逐渐滑落;(d)瞬态水凝胶粘合剂生物电子界面结合电极采集大鼠心电信号的示意图;(e)瞬态水凝胶粘合剂结合电极采集的大鼠心电(ECG)和脑电(EEG)信号与商用电极(CE)采集信号的信噪比(SNR)对比。
本研究创新地提出了一种自液化的水凝胶粘合剂,为解决传统水凝胶的难题打开了新思路,开拓了化学燃料驱动的瞬态自液化水凝胶粘合剂的应用新方向,为自脱除生物电子界面的开发开辟了新的途径,将有力地推动下一代具有类生命特性的非平衡水凝胶材料的应用。
吉林大学化学学院超分子结构与材料全国重点实验室李云峰教授与哈尔滨工业大学齐殿鹏教授为该文章的共同通讯作者,文章第一作者是吉林大学化学学院博士研究生李梦圆。该研究得到国家自然科学基金委的支持。
论文链接:
https://doi.org/10.1002/anie.202503010